Причины возникновения ожирения у детей
Детское ожирение влечет за собой очень неблагоприятные последствия, такие как сахарный диабет, сердечно-сосудистые заболевания, ортопедические проблемы и многое другое.
- Основной причиной развития избыточной массы жировой ткани в детском возрасте принято считать неправильную культуру питания. Многие родители из-за банальной неосведомленности составляют несбалансированный детский рацион. Как правило, пища такого ребенка обогащена избыточным количеством сахара. Также чрезмерное потребление фастфуда, высококалорийных продуктов (чипсы, хлебобулочные и кондитерские изделия) приводит к избыточному весу. Сладкие газированные напитки серьезно усугубляют ситуацию.
- Следующей и не менее важной причиной ожирения в детском возрасте является малоподвижный образ жизни ребенка. Физическая апатия рано или поздно приводит к избыточному весу. При отсутствии какой-либо физической нагрузки ребенок более стремительно будет набирать лишние килограммы. Родители должны следить за тем, чтобы ребенок меньше времени проводил перед телевизором, за компьютером, за телефоном. Родители должны обеспечить ребенка прогулками на свежем воздухе, подвижными играми. К тому же, пребывание на свежем воздухе положительно сказывается на умственных способностях.
- Третье место занимает генетическая предрасположенность. Если кто-то из членов семьи страдает избыточной массой тела, в этом случае у ребенка появляется дополнительный фактор риска. Если в доме всегда имеется высококалорийная пища в свободном доступе, а сам ребенок ведет малоподвижный образ жизни, риск очень возрастает.
- Психологические проблемы – следующий фактор, который влечет за собой развитие ожирения у детей. Это могут быть какие-либо проблемы внутри семьи или неурядицы с друзьями, особенно в подростковом периоде. Дети, как и взрослые, могут просто «заедать» проблемы, не замечая этого. В некоторых случаях отсутствие родительского внимания является причиной переедания.
СИМПТОМЫ И МЕДИЦИНСКАЯ КЛАССИФИКАЦИЯ ОЖИРЕНИЯ У ДЕТЕЙ
У грудных детей первые тревожные признаки проявляются в виде излишней массы тела, запоров и дисбактериоза, частых аллергий, инфекционных заболеваний. У детей постарше и подростков также отмечаются перечисленные симптомы, но при этом возникают и другие признаки:
- повышенное потоотделение, одышка, головокружение даже при минимальных нагрузках;
- отеки конечностей, боли в суставах;
- нарушение полового созревания, у девушек — сбои менструального цикла;
- быстрая утомляемость, подавленность, депрессивные состояния;
- повышение артериального давления;
- дефекты фигуры (заметно полные бедра, плечи, руки, живот).
По своей этиологии ожирение у детей и подростков делится на:
- первичное — алиментарное (А) и экзогенно-конституциональное (ЭК) — первое вызывается неправильным рационом, а второе — генетической предрасположенностью;
- вторичное, вызванное приобретенными и врожденными болезнями;
- смешанное, возникающее по причинам из обеих перечисленных выше категорий.
Также существует классификация детского ожирения по степени отклонения веса от нормы:
- 1 степень — масса тела выше нормы на 15–24%;
- 2 ст. — на 25–49%;
- 3 ст. — на 50–99%;
- 4 ст. — на 100%.
Кроме того, клиницисты могут классифицировать ожирение у детей и подростков на основании увеличения ИМТ (индекса массы тела), который измеряется в килограммах на квадратный метр:
- избыточный вес (предожирение) — ИМТ 25–30 кг/м2;
- начальная степень ожирения — ИМТ 30–35 кг/м2;
- среднетяжелая — 35–40 кг/м2;
- тяжелая — свыше 40 кг/м2.
В каждом конкретном случае клиническая картина отличается индивидуальным характером, поэтому лечение ожирения должно проводиться под квалифицированным врачебным контролем.
ПРИЧИНЫ ДЕТСКОГО ОЖИРЕНИЯ
Одним из наиболее вероятных факторов риска является наследственность — так называемый семейный синдром. При наличии ожирения у обоих родителей вероятность его возникновения у ребенка превышает 80%. Но при этом причиной ожирения могут стать и другие факторы, не имеющие отношения к наследственной предрасположенности.
Медики выделяют три критических периода развития ребенка, когда риск возникновения ожирения становится наиболее высоким:
- до 3 лет (первое наращивание жировой ткани в организме);
- 5–7 лет (второй период усиленного образования жировой ткани);
- 12–17 лет (полная перестройка организма в связи с половым созреванием и еще один период интенсивного образования жира).
Исходя из этого, причины, вызывающие ожирение (кроме наследственности), будут разными для каждого возраста риска. Возникновению патологии у новорожденных и малышей до 3 лет могут способствовать:
- неправильный рацион питания, перекармливание;
- ранний прикорм, искусственные смеси с высокой калорийностью;
- дефицит физической активности и другие.
В период с 5 до 7 лет вызвать ожирение могут:
- неправильный режим активности и отдыха;
- малоподвижный образ жизни;
- раннее половое созревание;
- неполноценное питание с преобладанием углеводов и жиров;
- стрессы.
У подростков 12–17 лет риск возникновения ожирения возрастает на фоне пубертатного периода. Сбои обмена веществ могут быть спровоцированы такими факторами:
- дисбаланс гормонов, в том числе нарушения функций надпочечников, щитовидной железы;
- поликистоз яичников у девушек, адипозогенитальная дистрофия у юношей;
- недосыпание, гиподинамия, неполноценное питание;
- прием гормональных препаратов, антидепрессантов и другие.
Для первичной диагностики ожирения необходимо проанализировать образ жизни ребенка, рацион его питания, физическую активность и особенности строения тела.
Опасность детского ожирения
ВОЗ связывает это состояние с повышенной вероятностью преждевременной смерти, а также инвалидностью в более старшем возрасте. У детей с ожирением в 2 раза чаще развивается слепота, в связи с ухудшением циркуляции крови. Половое созревание у таких ребят начинается в более раннем возрасте.
Также, ожирение у детей дает дополнительную нагрузку на опорно-двигательный аппарат и провоцирует развитие многих сопутствующих болезней.
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний) Ожирение относится к многофакторным заболеваниям, возникающим в результате определенного взаимодействия генетических и негенетических причин. Роль “наследственности“ в развитии ожирения доказывается разной частотой встречаемости данного заболевания в различных этнических группах и более высокой конкордантностью в развитии патологии у однояйцовых близнецов. Самый частый вид ожирения, связанный с избыточным поступлением калорий в условиях гиподинамии и наследственной предрасположенности — конституционально-экзогенное (простое, идиопатическое) ожирение. Наиболее масштабное на сегодняшний день исследование по изучению генетического влияния на величину ИМТ (Genetic Investigation of Anthropometric Traits-GIANT), основанное на геномном анализе ассоциаций, выявило 97 хромосомных участков, связанных с развитием ожирения. Суммарно аллели данных сегментов хромосом объясняют от 2,5 до 20% общей вариабельности ИМТ. Кроме того, сравнительный анализ результатов исследования отдельно для детей и взрослых показал обширное перекрытие аллелей риска для избыточной массы тела и ожирения во всех группах, так что на сегодняшний день нет молекулярно-генетического объяснения раннего и позднего дебюта ожирения. Таким образом, простое ожирение является полигенным заболеванием. Однако при этом, по современным представлениям, вклад каждого из генов в предрасположенность к ожирению относительно невелик. Перспективными выглядят современные исследования особенностей количественного и качественного развития самой жировой ткани как бурой, так и белой, гормонов и секретируемых ею активных веществ. С учетом особенностей развития современного общества среди основных факторов риска развития избыточной массы тела и ожирения можно выделить несбалансированное питание, дефицит физической активности, отсутствие режима питания и отдыха, эмоциональные нагрузки, влияние образования и семейных традиций, изменения микробиоценоза кишечника, социальные влияния (агрессивная реклама нездорового питания). Таким образом, несмотря на то, что конституционально-экзогенное ожирение является заболеванием с наследственной предрасположенностью, вероятность его развития и степень проявления во многом зависят от образа жизни и характера питания. Генетическая составляющая является определяющей для моногенных и некоторых синдромальных форм ожирения. Значительно реже ожирение в детском и подростковом возрасте связано с применением лекарственных препаратов (например, глюкокортикостероидов, антидепрессантов, нейролептиков (антипсихотиков), противоэпилептических препаратов) или наличием заболеваний (опухолей гипоталамуса и ствола мозга, лучевой терапией опухолей головного мозга и гемобластозов, травмой черепа, инсультом, гиперкортицизмом, гипотиреозом и др. нейроэндокринными заболеваниями, хромосомными нарушениями).
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний) Клиническая картина определяется этиопатогенетической формой ожирения. Самая многочисленная группа, на долю которой приходится до 98-99% всех случаев ожирения — простое (конституционально-экзогенное, идиопатическое) ожирение. Дебют заболевания чаще всего в возрасте после 5 лет, или в периоде полового созревания. Как правило, ожирение прогрессирует постепенно, на фоне хороших (часто ускоренных) темпов роста. Наличие стрий, фолликулярного кератоза, полифагии, черного акантоза, артериальной гипертензии и др. не всегда коррелирует со степенью ожирения. Характерно наличие избыточной массы тела и ожирения у родственников (родители, бабушки, дедушки).
Гипоталамическое ожирение в большинстве случаев отличается быстропрогрессирующим характером, развивается после оперативного вмешательства (лучевой терапии), реже — предшествует периоду постановки диагноза. В случае краниофарингиомы для большинства пациентов характерно замедление темпов роста; для глиом — симптомы преждевременного полового развития; неврологические жалобы (головные боли, нарушение зрения) зависят от локализации и прогрессии опухоли. У детей с гипоталамическим ожирением часто отмечаются нарушения ритма сна и бодрствования, и поведенческие нарушения. Следует особо отметить, что встречающийся в русскоязычной литературе и практике “гипоталамический синдром пубертатного периода” является не гипоталамическим ожирением, а простым конституционально-экзогенным ожирением с коморбидными состояниями.
При моногенных формах ожирение дебютирует в первые месяцы и годы жизни, для большинства синдромальных форм характерна задержка психомоторного развития.
- Скрининг на наличие моногенных и синдромальных форм ожирения рекомендуется детям с ранним (до 5 лет жизни) ожирением на фоне выраженной полифагии, особенно при наличии выраженного ожирения в семейном анамнезе.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).Синдромальные формы ожирения характеризуются ранним дебютом ожирения и его быстрым прогрессированием. Для большинства синдромальных форм характерна задержка нервно-психического развития от умеренной до тяжелой степени выраженности, наличие дисморфических признаков и органоспецифических аномалий развития. К настоящему времени изучено не менее 30 синдромов, ассоциированных с ожирением (наиболее известные приведены в табл. 1). Причинами синдромального ожирения могут быть мутации как одного (с. Альстрема, с. Коэна), так и нескольких генов (с. Барде-Бидля), хромосомные перестройки и/или патология импринтинга (с. Прадера-Вилли, наследственная остеодистрофия Олбрайта-Брайцева).
Синдром Прадера-Вилли (СПВ) является самой частой синдромальной формой ожирения и встречается у 1 из 10-30 тыс. новорожденных. Развитие СПВ обусловлено нарушением экспрессии генов отцовской аллели 15-й хромосомы (микроделеция, материнская дисомия, мутации центра импринтинга, хромосомные транслокации). Диагноз можно заподозрить еще пренатально по наличию сниженной двигательной активности плода, а неонатальная гипотония с отсутствием сосательного рефлекса, является настолько значимым клиническим признаком синдрома, что позволяет установить диагноз еще в роддоме, особенно в сочетании с характерными фенотипические стигмами (долихоцефалия, акромикрия, тонкие губы с опущенными вниз углами, миндалевидные глаза, страбизм) и признаками гипогонадизма (гипоплазия наружных половых органов, крипторхизм) у новорожденных. В неонатальном периоде из-за трудностей с кормлением дети с СПВ могут отставать в весе, тогда как с 2-х лет жизни отмечается второй характерный для синдрома период, сопровождающийся избыточным набором веса, повышенной заинтересованностью в пище, гиперфагией, приводящей к морбидному ожирению. Задержка психомоторного развития отмечается практически у всех детей с СПВ. Гипоталамическая дисфункция лежит в основе многих проявлений синдрома (гиперфагия, температурная, болевая дисрегуляция, эндокринопатии, включая дефицит гормона роста, гипогонадизм, гипотиреоз, надпочечниковую недостаточность центрального генеза). ДНК-метилирование при помощи метил-специфической полимеразной цепной реакции (ПЦР) является высоко специфичным методом исследования, позволяющим подтвердить или исключить диагноз СПВ.
Синдром Барде–Бидля (СББ) – аутосомно-рециссивное заболевание, характеризующееся ожирением, пигментным ретинитом, полидактилией, умственной отсталостью, гипогонадизмом и почечной патологией (аномалии развития почек, почечная недостаточность). По крайней мере 19 различных генов участвуют в развитии СББ, а также в развитии и функционировании цилий (первичных ресничек), которые в основном являются сенсорными органеллами и принимают участие в работе сигнальных путей, включая регуляцию пищевого поведения. СББ считается цилиопатией, а механизмы развития ожирения при СББ до сих пор изучаются.
Псевдогипопаратиреоз 1 А типа характеризуется сочетанием резистентности к паратгормону и специфическим фенотипом, названным наследственной остеодистрофией Олбрайта (НОО). НОО объединяет в себе специфические (брахидактилия, подкожные кальцинаты) и неспецифические проявления (ожирение, низкорослость, лунообразное лицо, умственная отсталость). Псевдогипопаратиреоз 1а типа развивается в результате нарушений пострецепторной передачи сигнала от рецептора к клетке и наиболее частой причиной являются инактивирующие мутации гена GNAS, приводящие к снижению экспрессии и функции стимулирующей α-субъединицы G белка (Gas). Заболевание характеризуется аутосомно-доминантным типом наследования. Ген GNAS импринтирован тканеспецифично и Gas образуется в ряде тканей (соматотрофах, гонадах, щитовидной железе, проксимальных почечных канальцах) только с материнского аллеля. В большинстве тканей Gas экспрессируется биаллельно, но даже 50% активности белка может быть недостаточно в некоторых тканях, поэтому развивается фенотип НОО. В силу этих особенностей экспрессии GNAS, если мутация унаследована от матери, то развивается как НОО, так и резистентность к паратгормону (ПТГ), также может отмечаться резистентность к ТТГ, гонадотропным гормонам и соматолиберину [80]. При инактивирующей мутации GNAS отцовской аллели экспрессия Gα с материнской аллели сохранена, поэтому, как правило, развиваются только специфические фенотипические признаки остеодистрофии Олбрайта (см. табл. 1).
Таблица 1 Синдромальные формы ожирения






Моногенные формы ожирения встречаются крайне редко, отличаются ранним дебютом (с первых месяцев жизни – до 1 года), полифагией. Для большинства пациентов характерно нормальное нервно-психическое развитие (см. табл. 2). Моногенные формы ожирения развиваются из-за мутации одного из генов, кодирующих белки лептин-меланокортиновой системы. Эта система является ключевой в регуляции пищевого поведения и энергетического обмена, активируется лептином (LEP), который секретируется адипоцитами, но свое действие оказывает через лептиновый рецептор (LEPR) аркуатных ядер гипоталамуса, приводя к активации проопиомеланокортина (ПОМК). Под воздействием фермента конвертазы прогормона 1 (КП1) из ПОМК образуются адренокортикотропный гормон (АКТГ) и α-меланоцитстимулирующий гормон (α-МСГ), который в свою очередь активирует рецептор МС4R в паравентрикулярных ядрах, что приводит к сигнализации о насыщении. Фермент КП 1 расщепляет прогормоны в парах основных аминокислот, оставляя С-терминальные основные остатки, которые удаляет карбоксипептидаза Е (КПЕ). Нейротрофический фактор головного мозга (BDNF) и его рецептор (TrkB) также участвуют в регуляции сигнального пути MC4R, а ген SIM 1 (single-minded homolog 1) кодирует транскрипционный фактор, участвующий в развитии супраоптичексих и паравентрикулярных ядер.
Таблица 2 Моногенные формы ожирения





Дефицит лептина Врожденный дефицит лептина — редкий синдром, характеризующийся морбидным ожирением с первых месяцев жизни на фоне выраженной гиперфагии и низким, неопределяемым уровнем лептина. Для этих пациентов характерен гипогонадотропный гипогонадизм, дефицит гормона роста, гипотиреоз центрального генеза, также дети с дефицитом лептина часто болеют респираторными инфекционными заболеваниями из-за гипофункции Т-клеток.
Дефицит рецептора лептина Характеризуется схожей с дефицитом лептина клинической картиной, однако отличительным лабораторным признаком этого синдрома является повышенное содержание лептина в сыворотке крови.
Дефицит ПОМК Сочетание быстропрогрессирующего морбидного ожирения, повышенного аппетита и надпочечниковой недостаточности с неопределяемыми в сыворотке крови уровнями кортизола и АКТГ характерны для дефицита проопиомеланокортина. Дефицит ПОМК приводит к гиперфагии и раннему развитию ожирения из-за потери передачи сигнала меланокортина на рецептор меланокортина-4 (MC4R). В постнатальном периоде жизни у новорожденного развивается надпочечниковая недостаточность (вторичная, из-за дефицита АКТГ, поскольку ПОМК — его предшественник) с характерной гипогликемией, длительной желтухой, предрасположенностью к тяжелым инфекциям. Из- за отсутствия воздействия меланоцитостимулирующего гормона (МСТ) на рецепторы меланокортина-1 у большинства таких детей бледная кожа и рыжие волосы.
Дефицит конвертазы прогормона 1 (КП 1) Мутации в этом ферменте приводят к нарушению расщепления множества прогормонов, таких как, прогонадотропин-рилизинг-гормон, проинсулин, протиротропин-рилизинг-гормон, ПОМК, способствуя развитию СТГ-дефицита, вторичного гипокортицизма, гипотиреоза, гипогонадизма. Неспособность расщеплять ПОМК — вероятный механизм развития ожирения у таких пациентов. Интестинальная дисфункция и постпрандиальная гипогликемия объясняются нарушением созревания гастрина, глюкагона, глюкагоно-подобного пептида-1 и инсулина (повышено содержание проинсулина) при дефиците КП 1.
Дефицит нейротрофического фактора головного мозга (BDNF) и его рецептора (TrkB) Развитие и дифференцировка нейронов центральной и периферической нервной системы зависит от нейротрофических факторов (нейротрофинов), которые секретируются тканями-мишенями. Сигналинг нейротрофинов осуществляется через специфическую активацию рецепторов тирозинкиназы В. Гетерозиготная мутация в гене NTRK2, кодирующего тирозинкиназу В (TrkB) была выявлена у 8-летнего мальчика с выраженной задержкой развития (снижение краткосрочной памяти, стереотипное поведение), нарушением болевой чувствительности и тяжелым ожирением.
Мутация в гене SIM1 De novo транслокация между 1-й и 6-й хромосомами была обнаружена у девочки, имевшей массу тела 47 кг в возрасте 5,5 лет [81]. Мутация приводит к разрыву в SIM1 гене, человеческом гомологе Drosophila Single-minded (Sim) гена, регулирующего нейрогенез. SIM1 ген кодирует транскрипционный фактор, вовлеченный в формирование паравентрикулярного и супраоптического ядер. Делеция области 6q16.2-6q16.3 выявлена у пациентов с ожирением и наличием фенотипа СПВ [82].
Дефицит MC4R Мутации гена MC4R — самая частая моногенная причина ожирения. Пациенты с дефицитом MC4R характеризуются повышенным аппетитом, ожирением в сочетании с высокими темпами роста. Наряду с избытком жировой массы при мутациях гена MC4R характерно увеличение количества тощей массы и минеральной плотности костей, поэтому такие люди часто кажутся «ширококостными». У больных с дефицитом MC4R отмечаются более высокие концентрации инсулина натощак по сравнению с детьми аналогичного возраста, пола и ИМТ. Гомозиготные мутации встречаются намного реже гетерозиготных, и отличаются более выраженной клинической симптоматикой [83]. У взрослых пациентов отмечается менее выраженная гиперфагия, гиперинсулинемия, чем у детей с аналогичной мутацией. Нейроэндокринные заболевания являются редкими причинами ожирения в детском возрасте и отличаются характерными клиническими признаками. Так, для гиперкортицизма характерно снижение темпов роста наряду с прогрессирующим ожирением, тогда как появления сухости кожных покровов, непереносимости холода, быстрой утомляемости может свидетельствовать о наличии гипотиреоза. Общие принципы дифференциальной диагностики различных форм ожирения представлены в приложении Б.
Диагностика
Диагностика заболевания или состояния
Критерии установления диагноза/состояния: В качестве диагностического критерия избыточной массы тела и ожирения у детей рекомендовано определение величины стандартных отклонений индекса массы тела (SDS ИМТ). С учетом рекомендаций ВОЗ, ожирение у детей и подростков от 0 до 19 лет следует определять, как ИМТ, равный или более +2,0 SDS ИМТ, а избыточную массу тела от +1,0 до +2,0 SDS ИМТ. Нормальная масса тела диагностируется при значениях ИМТ в пределах ± 1,0 SDS ИМТ [1, 8, 10]. На сайте ВОЗ представлены новые нормативные значения роста и веса для детей в виде таблиц и кривых для возраста 0 ― 5-ти лет (http://who.int/childgrowth/standards/ru/) и для возраста 5 ― 19 лет (http://who.int/growthref/who2007_bmi_for_age/en/index.html) (см. приложение Г1, Г2). Кроме этого, для диагностики избыточной массы тела и ожирения у детей могут использоваться программные средства ВОЗ Anthro (для возраста 0 – 5 лет) и AnthroPlus (для возраста 5 – 19 лет) для персональных компьютеров (http://who.int/childgrowth/software/en/). Поскольку непосредственно оценить количество жировой ткани в организме сложно, наиболее информативным является определение ИМТ, который рассчитывается как отношение массы тела в килограммах к квадрату роста человека, выраженному в метрах. Доказано, что ИМТ коррелирует с количеством жировой ткани в организме как у взрослых, так и у детей. Согласно критериям ВОЗ, у взрослых нормальной массе тела соответствует ИМТ 18,5—24,9, ИМТ 25—29,9 — избыточному весу, а ожирение диагностируется при ИМТ выше 30. Критерии избыточной массы тела у детей определяются по данным перцентильных таблиц или стандарных отклонений ИМТ (SDS — standard deviation score). В них учитывается не только рост, вес, но также пол и возраст ребенка. Это связано с тем, что значение ИМТ у детей меняется с развитием ребенка: от высокого в первый год жизни, сниженного в период раннего детства (2—5 лет) и постепенно увеличивающегося в период полового развития, что в целом отражает динамику жировой ткани. Данные нормативы объединяет общий принцип: перцентили должны быть симметричны относительно медианы (50-й перцентили). ВОЗ пользуется стандартными отклонениями –1, –2, –3 SDS, медиана и +1, +2, +3 SDS.
Жалобы и анамнез При сборе анамнеза выявляют вес при рождении, возраст дебюта ожирения, психомоторное развитие, наследственный анамнез по ожирению (включая рост и вес родителей), сахарному диабету 2 типа и сердечно-сосудистым заболеваниям, динамику роста и веса, наличие неврологических жалоб (головные боли, нарушение зрения).
Физикальное обследование
- Всем детям с ожирением и избыточной массой тела для определения наличия и степени ожирения рекомендуется проводить измерения роста, SDS роста, веса с расчетом SDS ИМТ, окружности талии, оценивать характер распределения подкожной жировой клетчатки [1, 10, 23, 45, 65].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
- Всем детям с ожирением и избыточной массой тела для выявления артериальной гипертензии рекомендуется проводить измерение артериального давления (АД) и оценивать его с учетом пола, возраста и роста [1, 11, 12, 23, 29]:
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
- Для диагностики наличия артериальной гипертензии, выявленной при обычном измерении, рекомендуется проведение суточного мониторирования АД [11, 12, 23, 30].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).Комментарии:Измерение и последующая оценка артериального давления (АД) проводится согласно “Клиническим рекомендациям по артериальной гипертензии у детей” МЗ РФ и рекомендациям по профилактике сердечно-сосудистых заболеваний в детском и подростковом возрасте, разработанными экспертами ассоциаций детских кардиологов России и педиатров России [11,12].У детей и подростков выделяют: нормальное АД, высокое нормальное АД и артериальную гипертензию 1 и 2 степени. Оценка уровней АД проводится с использованием перцентильных таблиц, учитывающих пол, возраст и рост пациентовНормальное АД – систолическое (САД) и диастолическое артериальное давление (ДАД), уровень которого ≥10-го и <90-го процентиля кривой распределения АД в популяции для соответствующего возраста, пола и роста.Высокое нормальное АД – САД и/или ДАД, уровень которого ≥90-го и <95-го процентиля кривой распределения АД в популяции для соответствующего возраста, пола и роста или ≥120/80 мм рт.ст. (даже если это значение <90-го процентиля).Артериальная гипертензия определяется как состояние, при котором средний уровень САД и/или ДАД, рассчитанный на основании трех отдельных измерений ≥значения 95-го процентиля кривой распределения АД в популяции для соответствующего возраста, пола и роста.Если уровни САД и ДАД попадают в разные категории, то степень АГ устанавливается по более высокому значению одного из этих показателей.У детей и подростков выделяют 2 степени АГ:
1 степень – средние уровни САД и/или ДАД из трех измерений равные или превышающие значения 95-го процентиля, установленные для данной возрастной группы, при условии, что они превышают 99-й процентиль не более чем на 5 мм рт.ст.2 степень (тяжелая) – средние уровни САД и/или ДАД из трех измерений, превышающие значения 99-го процентиля более чем на 5 мм рт.ст., установленные для данной возрастной группы.
- Всем детям с ожирением и избыточной массой тела для скрининга ассоциированных с ожирением заболеваний рекомендуется определять наличие и характер стрий, фолликулярного кератоза, acanthosis nigricans, андрогензависимой дермопатии (у девочек – гирсутим, акне, жирная себорея) [1, 23, 29, 45]:
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
- Всем детям с ожирением и избыточной массой тела для объективной оценки состояния ребенка рекомендуется оценивать стадию полового развития по шкале Таннера (Приложение Г3) [1, 23, 29, 45]:
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
- Всем детям с ожирением и избыточной массой тела для выявления генетических синдромов, ассоциированных с ожирением, рекомендуется выявлять характерные специфические фенотипические особенности (см. табл. 2) [1, 23, 29, 65]:
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Лабораторные диагностические исследования
- Всем пациентам с ожирением с целью скрининга осложнений рекомендовано исследование биохимического анализа крови для выявления нарушений липидного обмена, определение активности аланинаминотрансферазы (АлАТ) и аспартатаминотрансферазы (АсАТ) в крови в сочетании с ультразвуковым исследованием органов брюшной полости (печени) [11,12, 16, 23, 30, 66].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).Комментарии:Для диагностики дислипидемии у всех определяют уровень общего холестерина, уровни холестерина липопротеидов высокой и низкой плотности, триглицеридов в крови.Диагноз дислипидемии устанавливается при наличии 2-х и более “высоких” и/или “низких” показателей: Холестерин 5,2 ммоль/л Триглицериды >1,3 (для детей до 10 лет); 1,7 (для детей старше 10 лет) ммоль/л ЛПВП* ≤ 0,9 (мальчики) и ≤ 1,03 (девочки) ммоль/л ЛПНП* 3,0 ммоль/л* Уровни холестерина липопротеидов высокой и низкой плотностиТакже установлены критерии оптимальных, повышенных, высоких и низких значений липидов, липопротеидов и аполипопротеинов у детей и подростков (см. табл. 1)
Таблица 3 Классификация уровней липидов, липопротеидов и аполипопротеинов (апо) сыворотки крови у детей и подростков [13,14]
Исследование активности АлАТ и АсАТ в сочетании с ультразвуковым исследованием печени рекомендуется всем пациентам с ожирением для скрининга неалкогольной жировой болезни печени. Жировой гепатоз имеют 25-45% подростков с ожирением; с длительностью ожирения может прогрессировать и поражение печени: стеатогепатит, фиброз, цирроз. Так, в США неалкогольная жировая болезнь печени является наиболее частой причиной развития цирроза у подростков и самой частой причиной для трансплантации печени у взрослых [15].Активность АлАТ, превышающая верхнюю границу нормы, установленной для данной лаборатории, у детей с признаками НАЖБП по УЗИ при отсутствии других причин синдрома цитолиза (вирусные, метаболические поражения печени и др.) расценивается как проявление стеатогепатита [16]. В сомнительных случаях достоверная диагностика неалкогольного стеатогепатита возможна только после морфологического исследования ткани печени.
- Всем пациентам с ожирением старше 10 лет для выявления нарушений углеводного обмена рекомендовано проведение глюкозотолерантного теста (ОГТТ) с определением глюкозы натощак и через 120 минут [67, 68, 69].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).Комментарии:Условия проведения теста: утром натощак, на фоне 8-14 часового голодания, пациент выпивает глюкозу из расчета 1,75 г сухого вещества на 1 кг веса, но не более 75 г, разведенную в 250 мл воды. В течение трех дней до проведения пробы пациенту рекомендуется прием пищи с содержанием углеводов не менее 250—300 г/сутки и обычная физическая активность.Оценка ОГТТ теста (проводится по уровню глюкозы плазмы крови): Нормогликемия – это уровень глюкозы натощак менее 6,1 ммоль/л и уровень глюкозы через 2 часа стандартного ПГТТ менее 7,8 ммоль/л. Нарушение гликемии натощак: уровень глюкозы натощак составляет 6,1 – 6,9 ммоль/л; Нарушение толерантности к глюкозе: уровень глюкозы через 2 часа ОГТТ соответствует 7,8 – 11,1 ммоль/л.
Диагноз СД у детей выставляется если1. Уровень глюкозы натощак 7,0 ммоль/л; состояние натощак определяется как отсутствие потребления калорий в течение, по крайней мере, 8 ч.a или 2. Уровень гликемии через 2 часа стандартного ОГТТ 11,1 ммоль/л, или3. Имеются классические симптомы сахарного диабета (полиурия, полидипсия, необъяснимое снижение веса) в сочетании со случайным определением гликемии крови 11,1 ммоль/л. “Случайным” считается измерение уровня глюкозы в любое время дня без взаимосвязи со временем приема пищи, или4. Гликированный гемоглобин (HbA1c) > 6,5% b. Исследование рекомендуется проводить в сертифицированной лаборатории (с использованием метода, одобренного Национальной программой стандартизации гликогемоглобина (National Glycohemoglobin Stadardization Program) и стандартизированного в соответствии с исследованием по контролю за диабетом и его осложнениями (DCCT — Diabetes Control and Complications Trial).a — При отсутствии явной гипергликемии диагноз СД, поставленный на основании этих критериев, необходимо подтверждать повторными тестами.b — Уровень менее 6,5% не исключает возможности диагностики СД по уровню глюкозы.
Не целесообразно исследование уровня глюкозы в крови с помощью глюкометров для диагностики нарушений углеводного обмена, так как глюкометры не обладают достаточной точностью для убедительной постановки диагноза и могут привести к ошибкам при диагностике [67].При клинически манифестном СД проводить ОГТТ не рекомендуется, нарушения углеводного обмена можно диагностировать с помощью показателей гликемии натощак, постпрандиально или в течение дня, исследованием уровня гликированного гемоглобина.Проведение ОГТТ детям с ожирением, не достигших 10 лет, показано при наличии у ребенка дополнительных факторов риска: клинических признаков инсулинорезистентности (акантоз), гестационного диабета у матери, СД у родственников 1-й и 2-й линии родства, при подозрении на врожденные синдромы, связанные с ранним развитием СД и др. и в каждом случае решается индивидуально [68].Согласно эпидемиологическим исследованиям, лица с нарушением гликемии натощак и нарушением толерантности к глюкозе составляют группу риска по развитию сахарного диабета 2 типа, а данные нарушения углеводного обмена расцениваются как “предиабет”.
Инструментальные диагностические исследования
- Для скрининга НАЖБП и желчнокаменной болезни у детей и подростков с ожирением рекомендовано проведение ультразвукового исследования органов брюшной полости (комплексного) [1, 15, 16, 66, 76].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).Комментарии:Инструментальные методы исследования являются ведущими в установлении диагноза НАЖБП и желчнокаменной болезни. Ультразвуковое исследование помогает выявить стеатоз печени и наличие калькулезного холецистита с достаточно высокой точностью. Диагностическими ультразвуковыми признаками жирового гепатоза являются гепатомегалия, неоднородность паренхимы и ослабление ультразвукового сигнала в дистальных отделах печени, обеднение сосудистого рисунка.«Золотым стандартом» диагностики НАЖБП является чрескожная биопсия печени под контролем ультразвукового исследования. Однако ее широкое использование, особенно в педиатрической практике ограничено ввиду инвазивности методики.
- Проведение ночной полисомнографии рекомендуется детям и подросткам с ожирением при клинических признаках синдрома обструктивного апноэ во сне: повышенная сонливость в дневное время, храп во время сна, остановки дыхания во время сна [1, 23, 29, 70].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).Комментарии:Синдром обструктивного апноэ во сне характеризуется нарушением дыхания во время сна в виде длительной частичной обструкции верхних дыхательных путей и (или) полной интермиттирующей обструкции (обструктивное апноэ), что вызывает нарушение нормальной легочной вентиляции во сне и качество сна. Избыточное отложение жировой ткани в области глотки, шеи, грудной клетки, брюшной полости, инфильтрация диафрагмы жировой тканью, повышенная миорелаксация во сне, гипертрофия миндалин и аденоидов приводят к развитию синдрома обструктивного апноэ во сне. Частота этого синдрома у детей с избыточной массой тела и ожирением достигает 38% по сравнению с 3% в общей популяции. Ночная полисомнография является «золотым стандартом» диагностики обструктивного апноэ во сне.
Иные диагностические исследования
- Всем детям и подросткам с ожирением и избыточной массой тела рекомендуется проводить оценку фактического питания с использованием метода 24-часового (суточного) воспроизведения питания с помощью пищевого дневника для назначения диетотерапии или ее коррекции [23, 29].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).Комментарии: Оценка статуса питания имеет большую клиническую значимость, так как способствует своевременному выявлению групп риска по развитию ожирения и избыточной массы тела, а также других заболеваний, обусловленных неправильным питанием. Изучение пищевого статуса в клинической практике у детей и подростков полезно как при выборе, так и при оценке эффективности диетотерапии и фармакотерапии.Для оценки фактического питания и изменений пищевого статуса используются различные методы, в том числе, метод 24-часового (суточного) воспроизведения питания(ведение пищевого дневника) и метод анализа частоты потребления пищи.Метод регистрации потребляемой пищи посредствам пищевого дневника является наиболее точным и достоверным в оценке фактического питания. К его недостаткам можно отнести трудоемкость метода и влияние на привычное питание пациента.
- Проведение дополнительных исследований (исследование гормонального профиля, МРТ головного мозга, молекулярно-генетические и цитогенетические методы) у детей и подростков с ожирением рекомендовано только при подозрении на гипоталамическую, синдромальную, эндокринную или моногенную формы ожирения [1, 12, 23, 29].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).Комментарии:Гормональные исследования проводятся строго по показаниям.Исследования уровня тиреотропного гормона (ТТГ) в крови и уровня свободного тироксина (СТ4) сыворотки крови целесообразно при подозрении на гипотиреоз; исследование уровня общего кортизола сыворотки крови, исследование уровня адренокортикотропного гормона (АКТГ) в крови и исследование уровня лептина в крови — при подозрении на моногенное ожирение, связанное с дефицитом проопиомеланокортина, лептина; исследование уровней кортизола и АКТГ в крови, суточного ритма их секреции, исследование уровня свободного кортизола в моче, супрессивные тесты с дексаметазоном при подозрении на эндогенный гиперкортизицм; исследование уровня паратиреоидного гормона, проинсулина в крови – при подозрении на синдромальные формы ожирения – псевдогипопаратиреоз, дефицит проконвертазы 1 типа.Исследование уровня инсулиноподобного ростового фактора I в крови (ИРФ1) в крови показано при подозрении на гипоталамическое ожирение. Исследование уровня пролактина в крови показано при подозрении на гипоталамическое ожирение, а также при нарушении менструального цикла у девочек. Исследование уровней лютеинизирующего гормона в сыворотке крови, фолликулостимулирующего гормона в сыворотке крови, общего тестостерона, исследование уровня глобулина, связывающего половые гормоны, исследование уровня антимюллерова гормона в крови проводится при синдроме гиперандрогении, дисменорее у девочек и нарушениях полового развития у мальчиков.Исследование уровня альдостерона в крови, уровня ренина в крови, исследование уровней метанефринов и норметанефринов в моче показано для уточнения генеза впервые выявленной при обследовании пациента с ожирением артериальной гипертензии в зависимости от клинических проявлений.При подозрении на гипоталамическое ожирение показано проведение МРТ головного мозга.Определение мутаций в генах, цитогенетическое исследование (кариотип) проводятся при подозрении на моногенное ожирение и синдромальные формы. Особенностью синдромальных форм ожирения является наличие выраженной неврологической симптоматики – задержка психомоторного развития, сниженный интеллект и др. В данном случае желательна консультация врача-невролога, врача-генетика, проведение генетических исследований с учетом клинической картины и фенотипических особенностей.
- Консультации профильных специалистов (врача-кардиолога, врача-акушера-гинеколога, врача-офтальмолога, медицинского психолога, врача-психиатра и др.) рекомендованы детям и подросткам с избыточной массой тела и ожирением при выявлении профильных сопутствующих заболеваний ― артериальной гипертензии, нарушений менструального цикла, депрессии и др. [1, 12, 23, 29].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
- Оценка инсулинорезистентности (ИР) у детей и подростков с ожирением проводится по строгим показаниям и не рекомендуется в рутинной клинической практике [1, 23, 29].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).Комментарии:«Золотым стандартом» диагностики ИР являются эугликемический и гипергликемический клэмп, а также внутривенный глюкозотолерантный тест с частыми заборами крови, оцениваемый с помощью минимальной модели Бергмана [26,27].К сожалению, эти тесты неприменимы в повседневной практике, так как они весьма продолжительны, дорогостоящи и инвазивны, требуют специально обученного медицинского персонала и сложной статистической обработки результатов.В повседневной практике для оценки ИР при ожирении у детей и подростков наибольшей диагностической значимостью обладают значения стимулированного выброса инсулина и индекса Matsuda, определяемые по данным глюкозотолерантного теста [28]. Для уменьшения инвазивности исследования и снижения риска гемолиза предпочтительна установка внутривенного катетера. Исследование концентраций иммунореактивного инсулина (ИРИ) и глюкозы в крови проводится натощак, а также через 30, 60, 90 и 120 минут после нагрузки глюкозой с расчетом индекса Matsuda_Matsuda=10000/√(ИРИ0 х Гл0 х ИРИсред х Глсред),где ИРИ — иммунореактивный инсулин, мкЕд/мл; Гл — глюкоза, мг/%. ИРИ0, Гл0 — инсулин и глюкоза плазмы натощак; ИРИсред, Глсред — средний уровень инсулина и глюкозы при проведении ОГТТ. Значения индекса ниже 2,6 свидетельствуют о наличие инсулинорезистентности [64, 71].Следует отметить, что ввиду спорности оценки ИР, а также отсутствия на сегодняшний день официально разрешенной эффективной медикаментозной терапии данного состояния, оценка инсулинорезистентности должна проводиться по показаниям и не является обязательной в рутинной клинической практике. К показаниям для проведения глюкозотолерантного теста с оценкой ИР можно отнести наличие у пациента ранее выявленных нарушений углеводного обмена, отягощенный семейный анамнез (по СД 2 типа, гиперандрогении и др.), наличие объективных маркеров инсулинорезистентности — acanthosis nigricans или выраженная гиперпигментация кожных складок шеи, подмышечных или паховой областей, клинические признаки гиперандрогени.
- Детям и подросткам с ожирением и избыточной массой тела рекомендуется, по возможности, определение процентного соотношения воды, мышечной и жировой ткани с помощью анализатора состава тела человека [17, 18, 19-23, 74].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).Комментарии:Биоимпедансный анализ состава тела основан на измерении электрического сопротивления тканей (импеданса) при прохождении через них низкоинтенсивного электрического тока и позволяет оценить количество жировой и тощей массы, а также воды в организме (композиционный состав тела). По точности получаемых результатов биоимпедансный анализ приближается к данным, полученным при проведении рентгеновской денситометрии. Преимуществами метода являются отсутствие лучевой нагрузки и возможность проведения исследований в динамике. Существуют нормативы для оценки исследуемых параметров состава тела в зависимости от пола, возраста и этнической принадлежности, а также вида используемого анализатора [17,18].Исследование целесообразно для поддержания мотивационной приверженности пациента к лечению, оценке изменения композиционных параметров тела в динамике, но не является обязательным.
- Для персонификации проводимой диетотерапии детям и подросткам с ожирением и избыточной массой тела целесообразно, по возможности, исследование основного обмена с помощью метода непрямой респираторной калориметрии [24, 25].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).Комментарии:С целью повышения эффективности лечения ожирения у детей и подростков диетологами активно используется определение энерготрат покоя и метаболизма макронутриентов, которые относится к ведущим составляющим персонифицированной диетотерапии. Основным методом исследования основного обмена в настоящее время является непрямая респираторная калориметрия. Данная методика рекомендована Американской ассоциацией диетологов и нутрициологов и Американской академией педиатрии в качестве предпочтительного метода для оценки основного обмена у детей и подростков.Вместе с тем, учитывая дороговизну метода, необходимость дополнительного обучения врача проведению данного исследования, оценка основного обмена возможна на базе крупных центров с наличием специализированного эндокринологического отделения; не является обязательной.
Нормы суточного объема пищи
| Возраст ребенка | Объем суточного рациона (мл) |
| 1 — 1,5 года | 1000 — 1100 |
| 1,5 — 3 года | 1200 — 1300 |
| 3 — 5 лет | 1300 — 1500 |
| 5 — 7 лет | 1600 — 1800 |
| 7 — 11 лет | 2000 — 2200 |
| 11 — 15 лет | 2300 — 2500 |
Какие продукты нужно ограничить, правило «пищевого светофора»
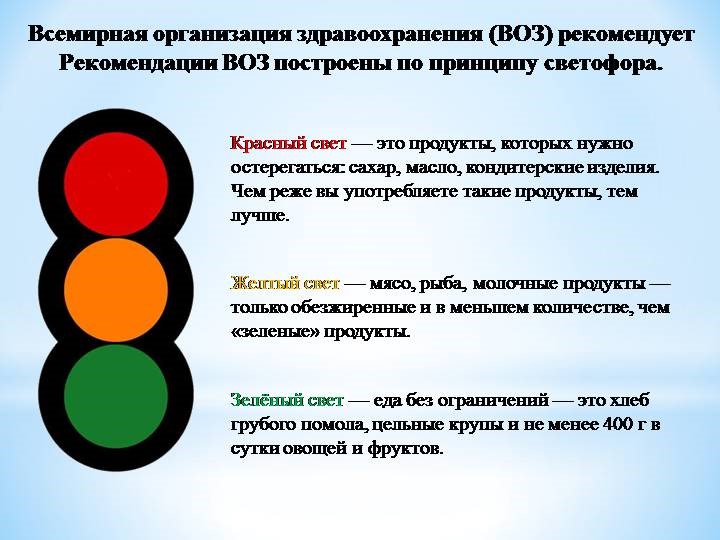
Наилучшим подходом к питанию детей с ожирением является метод «пищевого светофора».
Суть метода сводится к преимущественному употреблению продуктов, обладающих низкой калорийностью.
Суточная калорийность рациона составляет 1200 ккал, с последующим повышением.
Продукты делятся на три категории: «зеленые»,«желтые» и «красные».
Низкокалорийные продукты (большинство овощей и фруктов) считаются «зелеными» и рекомендуются к частому употреблению:
| 1. Капуста 2. Зеленые салаты 3. Огурцы 4. Томаты 5. Патиссоны 6. Баклажаны 7. Морковь 8. Зелень 9. Яблоки 10. Цитрусовые 11. Клубника и смородина 12. Оливковое масло 13. Морепродукты 14. Отварная рыба 15. Нежирные йогурты 16. Кефир, простокваша, айран 17 Яйца вареные «в мешочек» (до 2 штук) |
Продукты умеренной калорийности(например, злаки) считаются «желтыми», и их применение ограничивается.
| 1. Макароны из твердых сортов пшеницы 2. Каши на воде (кроме манной) 3. Выпечка из несладкого слоеного теста 4. Отварной картофель 5. Нежирные мясопродукты 6. Вареная колбаса 7. Горький шоколад 8. Пастила и мармелад, зефир 9. Твердый сыр 10. Творог 11. Сладкие фрукты и сухофрукты 12. Пряности 13. Кетчуп и соления 14. Чай |
«Красные» высококалорийные продукты подлежат резкому ограничению.
| 1. Фастфуд 2. Майонез 3. Плавленый сыр 4. Жирная сметана 5. Жирное мясо (свинина, жирная птица) 6. Копчености 7. Торты и пирожные с кремом и маслом 8. Дрожжевая выпечка 9. Белый хлеб 10. Газированные и сладкие напитки |
Дополнительные рекомендации
Следует максимально исключить из рациона фастфуд, майонезные заправки и соусы (предпочтение отдавать сметане низкой жирности или натуральному йогурту), сдобу. Из сладостей лучше выбирать зефир, пастилу, мармелад. Это не означает, что если ребенок пойдет на день рождения, то будет вынужден сидеть в сторонке от сверстников и уныло жевать салат с паровыми котлетами. Как и в любой системе питания, погрешности допустимы, важно чтобы «праздник живота» был редким явлением, в противном случае все труды пойдут насмарку.
Не стоит забывать, что все рекомендации по диетическому питанию для детей являются общими. Для того, чтобы подобрать индивидуальную программу питания для борьбы с избыточным весом или любой из степеней ожирения — необходимо проконсультироваться с врачом эндокринологом или диетологом.
Профилактика
Предупреждение эпидемии ожирения среди детей – это задача, требующая интеграции усилий родителей, представителей медицинского сообщества и сферы образования. Первым шагом на этом пути должно стать понимание родителями важности рационального питания в детском возрасте, воспитание правильных пищевых пристрастий у детей, организация режима дня ребенка с обязательным включением прогулок на свежем воздухе.
Другим важным моментом профилактики ожирения у детей служит привитие интереса к физической культуре, доступность занятий спортом в школе и по месту жительства. Важно, чтобы родители являли собой пример здорового образа жизни, а не авторитарно требовали его соблюдения от ребенка. Необходима разработка скрининговых программ по выявлению ожирения и его осложнений среди детей и подростков.
- https://russianberezka.ru/med-tips/problema-detskogo-ozhireniya-i-ego-profilaktika.html
- https://oxford-med.com.ua/media-center/publikacii/ozhirenie-u-detey-prichiny-i-lechenie/
- https://kikhtieva.com.ua/detskoe-ojireniye/
- https://diseases.medelement.com/disease/%D0%BE%D0%B6%D0%B8%D1%80%D0%B5%D0%BD%D0%B8%D0%B5-%D1%83-%D0%B4%D0%B5%D1%82%D0%B5%D0%B9-%D0%BA%D0%BF-%D1%80%D1%84-2021/16675
- https://www.deti-endo.ru/pravilnoe-pitanie-pri-ozhirenii-u-detej-i-podrostkov/
- https://a-mediya.ru/articles/dieta-dlya-detey
- https://www.KrasotaiMedicina.ru/diseases/children/obesity
 Go hydet
Go hydet 




